Purificação do sangue
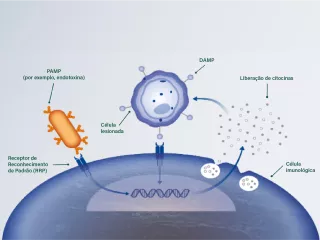
A única terapia capaz de remover eficazmente mediadores inflamatórios, padrões moleculares associados a danos (damage-associated molecular patterns, DAMPs) e/ou padrões moleculares associados a patógenos (pathogen-associated molecular patterns, PAMPs) (por exemplo, endotoxina).
Padrões moleculares associados a patógenos (PAMPs)
Todos os agentes patogênicos apresentam componentes específicos em sua superfície, conhecidos como PAMPs (por exemplo, endotoxina).1
Padrões moleculares associados a danos (DAMPs)
Quando as células hospedeiras são danificadas, elas liberam moléculas endógenas conhecidas como DAMPs, tais como trifosfato de adenosina (ATP), ácido desoxirribonucleico mitocondrial (DNA) e proteína de alta mobilidade do grupo 1 (HMGB1).2,3
Mediadores inflamatórios, como citocinas
Os mediadores inflamatórios são moléculas de sinalização fundamentais que regulam a resposta inflamatória, incluindo citocinas pró e anti-inflamatórias, por exemplo, interleucina (IL)-6, IL-8, IL-10 e fator de necrose tumoral (TNF)-α.4
Infecções, traumas, doenças agudas e certas intervenções terapêuticas podem estar associadas a uma resposta desregulada dos mediadores inflamatórios. Os pacientes podem incluir aqueles com4-10:
- Sepse/choque séptico
- COVID-19 grave
- Síndrome da angústia respiratória aguda (SDRA)
- Pancreatite aguda grave
- Insuficiência hepática aguda e aguda sobre crônica
- Toxicidade associada à terapia com células T com receptor de antígeno quimérico (Chimeric antigen receptor, CAR)
- Síndrome da resposta inflamatória sistêmica (SIRS) devido a queimaduras graves ou trauma
A sepse e o choque séptico estão associados a altas taxas de mortalidade e morbidade.
Sepse e choque séptico
- A análise dos dados do Estudo Global Burden of Diseases estimou que o número total anual de casos de sepse e choque séptico em 2017 foi de 48,9 milhões, levando a aproximadamente 11 milhões de mortes; isso representou cerca de 20% de todas as mortes em todo o mundo.11
- Níveis elevados de citocinas no plasma, particularmente IL-6, estão associados a um risco aumentado de mortalidade após admissão na UTI em pacientes com sepse ou choque séptico.12-15
- A alta atividade endotoxínica está associada a maior gravidade16-18 da doença e falência orgânica em pacientes com sepse/choque séptico.16
Disfunção multiorgânica
- A falência múltipla de órgãos foi relatada em cerca de 75% dos pacientes gravemente enfermos com sepse grave.19
- A insuficiência renal e respiratória combinada é comum em pacientes gravemente enfermos; cerca de 25% dos pacientes com COVID-19 grave que recebem suporte respiratório avançado também necessitam de suporte renal.20
- A disfunção/falência multiorgânica pode estar associada a um risco aumentado de mortalidade a curto e longo prazo,21-30 contribuindo para até 50% das mortes em UTI.21,22
COVID-19
- Em maio de 2022, a Organização Mundial da Saúde (OMS) registrou um total de >513 milhões de casos confirmados de COVID-19 em todo o mundo, incluindo >6 milhões de mortes.31
- Os mediadores inflamatórios, DAMPs e PAMPs, incluindo endotoxinas e partículas de SARS-CoV-2, são possíveis contribuintes para a falência multiorgânica em pacientes gravemente enfermos com COVID-19.5
A purificação do sangue é definida como o processo de remoção do sangue de mediadores e toxinas que podem causar patogênese.1,32
As terapias de purificação do sangue são concebidas para remover mediadores inflamatórios, PAMPs (tais como endotoxinas) e/ou DAMPs (tais como HMGB1) para combater os efeitos de um sistema imunitário desequilibrado.1,33
As evidências sugerem que o uso de terapias de purificação do sangue está associado a uma diminuição na dose/taxa de infusão de norepinefrina em pacientes com sepse ou choque séptico.34-38
Um estudo randomizado, cruzado e duplo-cego com pacientes com choque séptico e IRA relatou uma redução de 87% na taxa de infusão de norepinefrina em relação ao valor basal após 24 horas de tratamento com terapia de substituição renal contínua (CRRT) e terapia de purificação do sangue usando um conjunto de filtros adsorventes projetado para remover mediadores inflamatórios e endotoxinas (P = 0,02).38
As evidências sugerem que o uso de terapias de purificação do sangue está associado à melhora clínica da função orgânica (medida pela pontuação SOFA) em pacientes com COVID-19 grave, com ou sem IRA.39,40
Um estudo prospectivo, multicêntrico e observacional relatou uma melhora na função orgânica, medida pela pontuação SOFA (P = 0,002), em pacientes gravemente enfermos com COVID-19 grave tratados com terapia de purificação do sangue usando um conjunto de filtros adsorventes que removem mediadores inflamatórios e endotoxinas (um PAMP), bem como uma mortalidade observada menor em comparação com a mortalidade prevista, medida pela pontuação APACHE IV.39,40
A purificação do sangue tem o potencial de ajudar a mitigar a falência múltipla de órgãos e melhorar os resultados.34-42
A purificação do sangue é a única terapia capaz de remover eficazmente os mediadores inflamatórios, DAMPs e/ou PAMPs (por exemplo, endotoxina),1 o que pode ajudar a mitigar a falência multiorgânica e melhorar os resultados dos pacientes.34-42
Terapia de purificação do sangue para COVID-19
A conexão entre a COVID-19 e a sepse
Neste editorial, Jean-Louis Vincent, MD, PhD, professor de Medicina Intensiva na Université libre de Bruxelles, discute como a COVID-19 é uma resposta desregulada do hospedeiro à infecção.43
A COVID-19 pode afetar vários órgãos e tecidos44
- Cérebro: derrames, convulsões, confusão mental e inflamação cerebral
- Olhos e nariz: perda do olfato e conjuntivite
- Pulmões: destruição da parede celular dos alvéolos, diminuição da absorção de oxigênio; tosse, febre e dispneia
- Coração e vasos sanguíneos: coágulos sanguíneos, infarto do miocárdio e inflamação cardíaca
- Fígado: níveis enzimáticos anormais
- Rins: danos renais que podem resultar de infecção viral direta dos rins ou choque séptico
- Intestinos: ≥20% dos pacientes com diarreia
Informações importantes sobre segurança
Oxiris
Registro ANVISA: 80145240445
PrisMax/Thermax
Registro ANVISA: 80145240450
Bolsa Descartável Thermax
Notificação Anvisa: 80145249055
DRENO EXTENSOR AUTO-EFLUENTE
Notificação Anvisa: 80145240448
KIT AUTO-EFLUENTE
Notificação Anvisa: 80145240449
CE 0123
CE 2797
Vantive, Oxiris e PrisMax são marcas comerciais da Vantive Health LLC ou de suas afiliadas.
Referências
-
Monard C, Rimmelé T, Ronco C. Extracorporeal blood purification therapies for sepsis. Blood Purif. 2019;47(suppl 3):1-14.
-
Gotts JE, Matthay MA. Sepsis: pathophysiology and clinical management. BMJ. 2016;353:i1585.
-
Schaefer L. Complexity of danger: the diverse nature of damage-associated molecular patterns. J Biol Chem. 2014;289(51):35237-35245.
-
Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (Sepsis-3). JAMA. 2016;315(8):801-810.
-
Nadim MK, Forni LG, Mehta RL, et al. COVID-19-associated acute kidney injury: consensus report of the 25th Acute Disease Quality Initiative (ADQI) Workgroup. Nat Rev Nephrol. 2020;16(12):747-764.
-
Husain-Syed F, Slutsky AS, Ronco C. Lung-kidney cross-talk in the critically ill patient. Am J Respir Crit Care Med. 2016;194(4):402-414.
-
Shen Y, Cui N, Miao B, et al. Immune dysregulation in patients with severe acute pancreatitis. Inflammation. 2011;34:36-42.
-
Ilonen I, Koivusalo AM, Repo H, Höckerstedt K, Isoniemi H. Cytokine profiles in acute liver failure treated with albumin dialysis. Artif Organs. 2008;32(1):52-60.
-
Shimabukuro-Vornhagen A, Gödel P, Subklewe M, et al. Cytokine release syndrome. J Immunother Cancer. 2018;6:56.
-
Jeschke MG, van Baar ME, Choudhry MA, Chung KK, Gibran NS, Logsetty S. Burn injury. Nat Rev Dis Primers. 2020;6(1):11.
-
Rudd KE, Johnson SC, Agesa KM, et al. Global, regional, and national sepsis incidence and mortality, 1990-2017: analysis for the Global Burden of Disease Study. Lancet. 2020;395(10219):200-211.
-
Andaluz-Ojeda D, Bobillo F, Iglesias V, et al. A combined score of pro- and anti-inflammatory interleukins improves mortality prediction in severe sepsis. Cytokine. 2012;57(3):332-336.
-
Mat-Nor MB, Md Ralib A, Abdulah NZ, Pickering JW. The diagnostic ability of procalcitonin and interleukin-6 to differentiate infectious from noninfectious systemic inflammatory response syndrome and to predict mortality. J Crit Care. 2016;33:245-251.
-
Barre M, Behnes M, Hamed S, et al. Revisiting the prognostic value of monocyte chemotactic protein 1 and interleukin-6 in the sepsis-3 era. J Crit Care. 2018;43:21-28.
-
Bozza FA, Salluh JI, Japiassu AM, et al. Cytokine profiles as markers of disease severity in sepsis: a multiplex analysis. Crit Care. 2007;11(2):R49.
-
Biagioni E, Venturelli C, Klein DJ, et al. Endotoxin activity levels as a prediction tool for risk of deterioration in patients with sepsis not admitted to the intensive care unit: a pilot observational study. J Crit Care. 2013;28(5):612-617.
-
Ikeda T, Ikeda K, Suda S, et al.Usefulness of the endotoxin activity assay as a biomarker to assess the severity of endotoxemia in critically ill patients. Innate Immun. 2014;20:881-887.
-
Ikeda T, Kamohara H, Suda S, et al. Comparative evaluation of endotoxin activity level and various biomarkers for infection and outcome of icu-admitted patients. Biomedicines. 2019;7:47.
-
Blanco J, Muriel-Bombín A, Sagredo V, et al. Incidence, organ dysfunction and mortality in severe sepsis: a Spanish multicentre study. Crit Care. 2008;12(6):R158. doi:10.1186/cc7157.
-
ICNARC. ICNARC report on COVID-19 in critical care: England, Wales and Northern Ireland 08 April 2022. Accessed April 2022. Available at: https://www.icnarc.org/our-audit/audits/cmp/reports
-
Mayr VD, Dünser MW, Greil V, et al. Causes of death and determinants of outcome in critically ill patients. Crit Care. 2006;10(6):R154.
-
Orban JC, Walrave Y, Mongardon N, et al. Causes and characteristics of death in intensive care units: a prospective multicenter study. Anesthesiology. 2017;126(5):882-889.
-
Lie KC, Lau C, Chau NV, et al. Utility of SOFA score, management and outcomes of sepsis in Southeast Asia: a multinational multicenter prospective observational study. J Int Care. 2018;6:9.
-
Lone NI, Walsh TS.Impact of intensive care unit organ failures on mortality during the five years after a critical illness. Am J Respir Crit Care Med. 2012;186:640-647.
-
Jain A, Palta S, Saroa R, Palta A, Sama S, Gombar S. Sequential organ failure assessment scoring and prediction of patient's outcome in intensive care unit of a tertiary care hospital. J Anaesthesiol Clin Pharmacol. 2016;32(3):364-368.
-
Ferreira FL, Bota DP, Bross A, Mélot C, Vincent JL. Serial evaluation of the SOFA score to predict outcome in critically ill patients. JAMA. 2001;286(14):1754-1758.
-
Liu J, Zhang S, Wu Z, et al. Clinical outcomes of COVID-19 in Wuhan, China: a large cohort study. Ann Intensive Care. 2020;10:99.
-
Jin M, Lu Z, Zhang X, et al. Clinical characteristics and risk factors of fatal patients with COVID-19: a retrospective cohort study in Wuhan, China. BMC Infect Dis. 2021;21:951.
-
Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020;395(10229):1054-1062.
-
Juvé-Udina ME, Adamuz J, López-Jimenez MM, et al. Predicting patient acuity according to their main problem. J Nurs Manag. 2019;27(8):1845-1858.
-
WHO COVID-19 Dashboard. 2022. Accessed May 2022. Available at: https://www.covid19.who.int.
-
Rimmelé T, Kellum JA. Clinical review: blood purification for sepsis. Crit Care. 2011;15(1):205.
-
Malard B, Lambert C, Kellum JA. In vitro comparison of the adsorption of inflammatory mediators by blood purification devices. Intensive Care Med Exp. 2018;6(1):12.
-
Turani F, Barchetta R, Falco M, Busatti S, Weltertet L. Continuous renal replacement therapy with the adsorbing filter Oxiris in septic patients: a case series. Blood Purif. 2019;47(suppl 3):54-58.
-
Schwindenhammer V, Girardot T, Chaulier K, et al. oXiris® use in septic shock: experience of two french centres. Blood Purif. 2019;47:29-35.
-
Lumlertgul N, Srisawat N. The haemodynamic effects of Oxiris haemofilter in septic shock patients requiring renal support: a single-centre experience. Int J Artif Organs. 2020;44:17-24.
-
Hawchar F, László I, Öveges N, Trásy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: a proof of concept randomized, controlled pilot study. J Crit Care. 2019;49:172-178.
-
Broman ME, Hansson F, Vincent JL, Bodelsson M. Endotoxin and cytokine reducing properties of the Oxiris membrane in patients with septic shock: a randomized crossover double-blind study. PLoS One. 2019;14:e0220444.
-
Villa G, Romagnoli S, De Rosa S, et al. Blood purification therapy with a hemodiafilter featuring enhanced adsorptive properties for cytokine removal in patients presenting COVID-19: a pilot study. Crit Care. 2020;24:605.
-
Nassiri AA, Hakemi MS, Miri MM, Shahrami R, Koomleh AA, Sabaghian T. Blood purification with CytoSorb in critically ill COVID-19 patients: a case series of 26 patients. Artif Organs. 2021;45(11):1338-1347.
-
Cruz DN, Antonelli M, Fumagalli R, et al. Early use of polymyxin B hemoperfusion in abdominal septic shock: the EUPHAS randomized controlled trial. JAMA. 2009;301(23):2445-52.
-
Rosalia RA, Ugurov P, Neziri D, et al. Extracorporeal blood purification in moderate and severe COVID-19 patients: a prospective cohort study. Blood Purif. 2022;51:233-242.
-
Vincent JL. COVID-19: it's all about sepsis. Future Microbiol. 2021;16:131-133.
-
Wadman M, Couzin-Frankel J, Kaiser J, Matacicet C. A rampage through the body. Science. April 17, 2020. Accessed April 2020. Available at: https://www.science.org/content/article/how-does-coronavirus-kill-clinicians-trace-ferocious-rampage-through-body-brain-toes.