Apoiando o funcionamento dos rins com CRRT
Injúria renal aguda: cada paciente é diferente
A injúria renal aguda (IRA) é definida como uma diminuição abrupta da função renal que ocorre durante um período de 7 dias ou menos, abrangendo tanto a lesão direta do rim como a insuficiência aguda da função.8
A IRA é uma síndrome heterogênea8,9 associada a resultados clínicos desfavoráveis, sendo que cada paciente apresenta um perfil de risco e uma trajetória de progressão da doença únicos.10,11
As incidências relatadas variam
A incidência relatada de IRA entre pacientes em UTI varia de 0,5% a 78,7%12-14; até cerca de 25% desses pacientes podem necessitar de terapia de substituição renal (TSR).15-18
Risco de mortalidade
A IRA está associada a um risco aumentado de morbidade19-29 e mortalidade a curto e longo prazo.30-35
Progressão para DRC
A IRA está associada a um risco aumentado de progressão para doença renal crônica (DRC), incluindo doença renal em estágio terminal (ESRD).31,34,36
Estado hemodinâmico
Muitos médicos preferem a CRRT à Terapia Renal Intermitente para pacientes com IRA que apresentam instabilidade hemodinâmica.6,36,37
Gravidade da sobrecarga de líquidos
As diretrizes clínicas recomendam a CRRT em pacientes com aumento da pressão intracraniana ou edema cerebral generalizado causado por sobrecarga de líquidos.6
Sugerimos o uso da CRRT, em vez da TSR intermitente padrão, para pacientes hemodinamicamente instáveis. (Grau 2B)6
Diretriz de prática clínica da KDIGO para injúria renal aguda
A CRRT é a modalidade de TSR preferida para pacientes com IRA que necessitam de um controle preciso de fluidos ou que estão hemodinamicamente instáveis.
CRRT para um gerenciamento preciso de fluidos
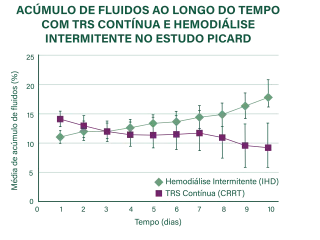
A CRRT demonstrou reduzir o acúmulo de fluidos de maneira eficaz e oportuna,37,38 proporcionando flexibilidade para ajustar a intensidade da remoção de fluidos a qualquer momento, de acordo com as mudanças na condição clínica do paciente.6
Evidências limitadas sugerem que a CRRT pode proporcionar um melhor controle da gestão de fluidos do que outras modalidades de TSR.6,38-40
Figura adaptada de Bouchard J, et al. Kidney Int. 2009;76(4):455-427. Os detalhes da coleta de dados e da análise estatística não foram relatados.
CRRT para pacientes com IRA que estão hemodinamicamente instáveis
A instabilidade hemodinâmica é comum entre pacientes gravemente enfermos com IRA submetidos a TSR (cerca de 36-70% dos pacientes)40,41 e pode estar associada a um risco aumentado de mortalidade e progressão da IRA. 42,43
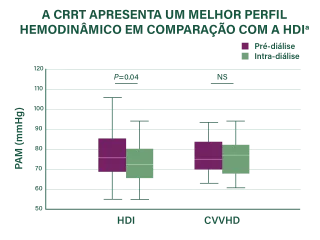
As evidências médicas existentes sugerem que a CRRT pode ser mais eficaz na manutenção da estabilidade hemodinâmica durante a remoção de líquidos, em comparação com a hemodiálise intermitente, HDi (intermittent hemodialysis, IHD) e a diálise sustentada de baixa eficiência (SLED).38,44-46
aUm ensaio clínico randomizado controlado com 80 pacientes adultos em estado crítico com insuficiência renal aguda que necessitavam de diálise em UTIs de uma instituição nos Estados Unidos (1995-1999). Os dados referem-se à terapia com HDi e CVVHD durante o primeiro dia de diálise. São apresentados os valores medianos com intervalo interquartil (bordas da caixa) e valores extremos (bigodes).38
A CRRT pode ser uma terapia econômica que pode proporcionar benefícios clínicos e operacionais adicionais para pacientes e hospitais.
Relação custo-benefício da CRRT
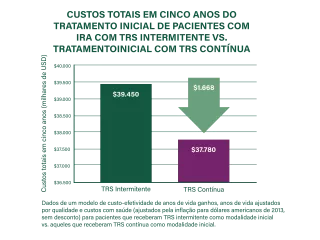
O tratamento inicial de pacientes com IRA utilizando CRRT pode ser mais econômico cinco anos após o início da TSR do que outras modalidades de TSR.3 Uma análise de custo descobriu que a CRRT pode economizar cerca de US$ 1.668 em cinco anos (com base no dólar americano de 2013).3,b,c
Análises de custo-benefício sugerem que a CRRT é mais econômica em comparação com a TSR intermitente, sendo a taxa de dependência da diálise o principal fator determinante da relação custo.47
bModelo de anos de vida ganhos, anos de vida ajustados pela qualidade e custos com cuidados de saúde (indexados ao dólar americano de 2013, sem desconto) para pacientes que receberam TSR intermitente como modalidade inicial em comparação com aqueles que receberam CRRT como modalidade inicial. Tanto para a CRRT inicial quanto para a TSR intermitente, a proporção dependente do tempo de sobreviventes de IRA que se tornaram dependentes de diálise foi ajustada a partir do estudo de Wald et al. (Crit Care Med. 2014; 42:868–877).3
cO modelo de custo levou em consideração apenas o custo da implementação da CRRT ou da TSR intermitente na UTI, o custo diário da independência da diálise e o custo diário da dependência da diálise no ambiente ambulatorial.3
Benefício do suporte orgânico integrado em um único sistema
A CRRT pode ser combinada com outras terapias de suporte orgânico em uma única plataforma, permitindo o tratamento integrado de pacientes com disfunção múltipla de órgãos.37
Um relatório consensual do 17º Grupo de Trabalho da Iniciativa de Qualidade em Doenças Agudas (Acute Disease Quality Initiative, ADQI) afirma que “em situações em que outras terapias extracorpóreas são necessárias, a CRRT é recomendada e os sistemas integrados são preferíveis aos sistemas paralelos”.37
Episódio 1: Decidir quando e quem deve iniciar a diálise aguda: Da evidência à prática clínica
Apresentado por Ravi Mehta, UC San Diego, com Marlies Ostermann, Guy’s and St. Thomas’ Foundation Trust
Episódio 2: Maximizando a vida útil do filtro durante a CRRT: Melhores práticas sobre anticoagulação e uso de citrato
Apresentado por Ravi Mehta, UC San Diego, com Ashita Tolwani, Universidade do Alabama em Birmingham
Episódio 3: Como desenvolver um programa de qualidade para cuidados de diálise aguda: Métricas de qualidade e melhoria contínua
Apresentado por Ravi Mehta, UC San Diego, com Theresa Mottes, Baylor College of Medicine
Informações importantes sobre segurança
PrisMax/Thermax
Registro ANVISA: 80145240450
Bolsa Descartável Thermax
Notificação Anvisa: 80145249055
DRENO EXTENSOR AUTO-EFLUENTE
Notificação Anvisa: 80145240448
KIT AUTO-EFLUENTE
Notificação Anvisa: 80145240449
Vantive, PrisMax são marcas comerciais da Vantive Health LLC ou de suas afiliadas.
Referências
-
Ostermann M, Joannidis M, Pani A, et al. Patient selection and timing of continuous renal replacement therapy. Blood Purif. 2016;42(3):224-237.
-
Acute Dialysis Quality Initiative (ADQI) 17 Workgroup. ADQI 17 Figures. 2016. Accessed July 8, 2024.
-
Koyner JL, Mackey RH, Echeverri J, et al. Dialysis dependence at 90 days post discharge for patients treated with continuous renal replacement therapy (CRRT) vs. intermittent hemodialysis (IHD). Poster presented at: 28th International Conference on Advances in Critical Care Nephrology – AKI & CRRT 2023; March 29 - April 1, 2023; San Diego, California, USA.
-
Naorungroj T, Neto AS, Wang A, Gallagher M, Bellomo R. Renal outcomes according to renal replacement therapy modality and treatment protocol in the ATN and RENAL trials. Crit Care. 2022;26:269.
-
Ethgen O, Schneider AG, Bagshaw SM, Bellomo R, Kellum JA. Economics of dialysis dependence following renal replacement therapy for critically ill acute kidney injury patients. Nephrol Dial Transplant. 2015;30(1):54-61.
-
Wald R, Gaudry S, da Costa BR, et al. Initiation of continuous renal replacement therapy versus intermittent hemodialysis in critically ill patients with severe acute kidney injury: a secondary analysis of STARRT-AKI trial. Intensive Care Med. 2023;49(11):1305-1316.
-
Ethgen O, Murugan R, Echeverri J, Blackowicz M, Harenski K, Ostermann M. Economic analysis of renal replacement therapy modality in acute kidney injury patients with fluid overload. Crit Care Explor. 2023;5(6):e0921.
-
KDIGO Acute Kidney Injury Work Group. KDIGO Clinical Practice Guideline for Acute Kidney Injury. Kidney Int Suppl. 2012;2(1):1-138.
-
Aglae C, Muller L, Reboul P, et al. Heterogeneity of cause, care, and prognosis in severe acute kidney injury in hospitalized patients: a prospective observational study. Can J Kidney Health Dis. 2019;6.
-
Cerdá J, Lameire N, Eggers P, et al. Epidemiology of acute kidney injury. Clin J Am Soc Nephrol. 2008;3(3):881-886.
-
Kellum JA, Sileanu FE, Bihorac A, Hoste EA, Chawla LS. Recovery after acute kidney injury. Am J Respir Crit Care Med. 2017;195(6):784-791.
-
Chawla L, Bellomo R, Bihorac A, et al. Acute kidney disease and renal recovery: consensus report of the Acute Disease Quality Initiative (ADQI) 16 Workgroup. Nat Rev Nephrol. 2017;13:241-257.
-
Mehta S, Chauhan K, Patel A, et al. The prognostic importance of duration of AKI: a systematic review and meta-analysis. BMC Nephrol. 2018;19(1):91.
-
Nisula S, Kaukonen KM, Vaara ST, et al. Incidence, risk factors and 90-day mortality of patients with acute kidney injury in Finnish intensive care units: the FINNAKI study. Intensive Care Med. 2013;39:420-428.
-
Melo FAF, Macedo E, Fonseca Bezerra AC, et al. A systematic review and meta-analysis of acute kidney injury in the intensive care units of developed and developing countries. PLoS One. 2020;15(1):e0226325.
-
Jiang L, Zhu Y, Luo X, et al. Epidemiology of acute kidney injury in intensive care units in Beijing: the multi-center BAKIT study. BMC Nephrol. 2019;20:468.
-
Bouchard J, Acharya A, Cerda J, et al. A prospective international multicenter study of AKI in the intensive care unit. Clin J Am Soc Nephrol. 2015;10(8):1324-1331.
-
Uchino S, Kellum JA, Bellomo R, et al. Acute renal failure in critically ill patients: a multinational, multicenter study. JAMA. 2005;294(7):813-818.
-
De Corte W, Dhondt A, Vanholder R, et al. Long-term outcome in ICU patients with acute kidney injury treated with renal replacement therapy: a prospective cohort study. Crit Care. 2016;20:256.
-
Garzotto F, Ostermann M, Martín-Langerwerf D, et al. The Dose Response Multicentre Investigation on Fluid Assessment (DoReMIFA) in critically ill patients. Crit Care. 2016; 20:196.
-
Gammelager H, Christiansen CF, Johansen MB, Tønnesen E, Jespersen B, Sørensen HT. Three-year risk of cardiovascular disease among intensive care patients with acute kidney injury: a population-based cohort study. Crit Care. 2014;18(5):492.
-
Go AS, Hsu C, Yang JT, et al. Acute kidney injury and risk of heart failure and atherosclerotic events. Clin J Am Soc Nephrol. 2018;13(6):833-841.
-
Wu V, Wu C, Huang T, et al. Long-term risk of coronary events after AKI. J Am Soc Nephrol. 2014;25(3):595-605.
-
Wu VC, Wu PC, Wu CH, et al. The impact of acute kidney injury on the long-term risk of stroke. J Am Heart Assoc. 2014;3(4):e000933.
-
Brown JR, Parikh C, Ross C, et al. Impact of perioperative acute kidney injury as a severity index for thirty-day readmission after cardiac surgery. Ann Thorac Surg. 2014;97(1)111-117.
-
Brown JR, Hisey W, Marshall E, et al. Acute kidney injury severity and long-term readmission and mortality after cardiac surgery. Ann Thorac Surg. 2016;102(5):1482-1489.
-
Lai TS, Wang CY, Pan SC, et al. Risk of developing severe sepsis after acute kidney injury: a population-based cohort study. Crit Care. 2013;17:R231.
-
Horkan CM, Purtle SW, Mendu ML, Moromizato T, Gibbons FK, Christopher KB. The association of acute kidney injury in the critically ill and postdischarge outcomes: a cohort study. Crit Care Med. 2015;43(2):354-364.
-
Koulouridis I, Price LL, Madias NE, Jaber BL. Hospital-acquired acute kidney injury and hospital readmission: a cohort study. Am. J. Kidney Dis. 2015;65(2)275-282.
-
Sawhney S, Marks A, Fluck N, et al. Acute kidney injury as an independent risk factor for unplanned 90-day hospital readmissions. BMC Nephrol. 2017;18:9.
-
Silver SA, Harel Z, McArthur E, et al. 30-day readmissions after an acute kidney injury hospitalization. Am J Med. 2017;130(2)163-172.
-
Coca SG, Yusuf B, Shlipak MG, Garg AX, Parikh CR. Long-term risk of mortality and other adverse outcomes after acute kidney injury: a systematic review and meta-analysis. Am J Kidney Dis. 2009; 53(6):961-973.
-
See EJ, Jayasinghe K, Glassford N, et al. Long-term risk of adverse outcomes after acute kidney injury: a systematic review and meta-analysis of cohort studies using consensus definitions of exposure. Kidney Int. 2019;95(1):160-172.
-
Srisawat N, Sileanu FE, Murugan R, et al. Variation in risk and mortality of acute kidney injury in critically ill patients: a multicenter study. Am J Nephrol. 2015;41(1):81-88.
-
Hoste EA, Bagshaw SM, Bellomo R, et al. Epidemiology of acute kidney injury in critically ill patients: the multinational AKI-EPI study. Intensive Care Med. 2015;41(8):1411-1423.
-
Coca SG, Singanamala S, Parikh CR. Chronic kidney disease after acute kidney injury: a systematic review and meta-analysis. Kidney Int. 2012;81(5):442-448.
-
Ronco C, Ricci Z, De Backer D, et al. Renal replacement therapy in acute kidney injury: controversy and consensus. Crit Care. 2015;19(1):146.
-
Nadim MK, Forni LG, Bihorac A, et al. Cardiac and vascular surgery-associated acute kidney injury: the 20th international consensus conference of the ADQI (Acute Disease Quality Initiative) group. J Am Heart Assoc. 2018;7(11):e008834.
-
Augustine JJ, Sandy D, Seifert TH, Paganini EP. A randomized controlled trial comparing intermittent with continuous dialysis in patients with ARF. Am J Kidney Dis. 2004;44(6):1000-1007.
-
Bouchard J, Soroko SB, Chertow GM, et al. Fluid accumulation, survival and recovery of kidney function in critically ill patients with acute kidney injury. Kidney Int. 2009;76(4):422-427.
-
Clark WR, Ding X, Qiu H, et al. Renal replacement therapy practices for patients with acute kidney injury in China. PLoS One. 2017;12(7):e0178509.
-
STARRT-AKI Investigators; Canadian Critical Care Trials Group; Australian and New Zealand Intensive Care Society Clinical Trials Group. Timing of initiation of renal-replacement therapy in acute kidney injury. N Engl J Med. 2020;383(5):502.
-
Izawa J, Kitamura T, Iwami T, et al. Early-phase cumulative hypotension duration and severe-stage progression in oliguric acute kidney injury with and without sepsis: an observational study. Crit Care. 2016;20:405.
-
Haase-Fielitz A, Haase M, Bellomo R, et al. Perioperative hemodynamic instability and fluid overload are associated with increasing acute kidney injury severity and worse outcome after cardiac surgery. Blood Purif. 2017;43(4):298-308.
-
Bagshaw SM, Berthiaume LR, Delaney A, Bellomo R. Continuous versus intermittent renal replacement therapy for critically ill patients with acute kidney injury: a meta-analysis. Crit Care Med. 2008;36(2):610-617.
-
Fieghen HE, Friedrich JO, Burns KE, et al. The hemodynamic tolerability and feasibility of sustained low efficiency dialysis in the management of critically ill patients with acute kidney injury. BMC Nephrol. 2010;11:32.
-
Singh A, Hussain S, Kher V, Palmer AJ, Jose M, Antony B. A systematic review of cost-effectiveness analyses of continuous versus intermittent renal replacement therapy in acute kidney injury. Expert Rev Pharmacoecon Outcomes Res. 2022;22(1):27-35.