Apoyo de la función renal con CRRT
Lesión renal aguda: cada paciente es diferente
La lesión renal aguda (LRA) se define como una disminución abrupta de la función renal que ocurre durante un período de 7 días o menos, y que abarca tanto la lesión renal directa como el deterioro agudo de la función.8
La LRA es un síndrome heterogéneo8,9 asociado a malos resultados de los pacientes, en que cada paciente tiene un perfil de riesgo y una trayectoria de progresión de la enfermedad únicos.10,11
Las incidencias informadas difieren
La incidencia notificada de LRA entre los pacientes de la UCI varía del 0,5% al 78,7%12-14; hasta ~25% de estos pacientes pueden requerir terapia de reemplazo renal (RRT).15-18
Riesgo de mortalidad
La LRA se asocia a un mayor riesgo de morbilidad19-29 y mortalidad a corto y largo plazo.30-35
Progresión a ERC
La LRA se asocia con un mayor riesgo de progresión a enfermedad renal crónica (ERC), que incluye la enfermedad renal en etapa terminal (ERET).31,34,36
Estado hemodinámico
Muchos médicos prefieren la CRRT a la IRRT para los pacientes con LRA que son hemodinámicamente inestables.6,36,37
Gravedad de la sobrecarga de fluido
Las directrices clínicas recomiendan la CRRT en pacientes con aumento de la presión intracraneal o edema cerebral generalizado causado por sobrecarga de fluidos.6
Sugerimos el uso de CRRT, en lugar de RRT intermitente estándar, para pacientes hemodinámicamente inestables. (Grado 2B)6
Directrices clínicas prácticas de KDIGO para lesión renal aguda
La CRRT es la modalidad de RRT preferida para los pacientes con LRA que requieren un control preciso de los fluidos o que son hemodinámicamente inestables.
CRRT para control preciso de fluidos
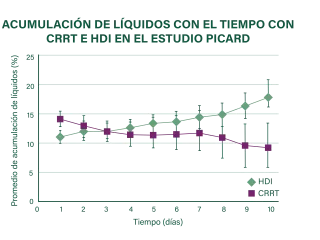
Se ha demostrado que la CRRT reduce la acumulación de fluido de manera efectiva y oportuna,37,38 proporcionando la flexibilidad para ajustar la intensidad de la eliminación de fluidos en cualquier momento de acuerdo con los cambios en el estado clínico del paciente.6
La evidencia limitada indica que la CRRT puede ser capaz de proporcionar un mejor control del tratamiento con fluidos que otras modalidades de RRT.6,38-40
Figura adaptada de Bouchard J, et al. Kidney Int. 2009;76(4):455-427. No se notificaron los detalles de la recopilación de datos ni del análisis estadístico.
CRRT para pacientes con LRA que son hemodinámicamente inestables
La inestabilidad hemodinámica es frecuente entre los pacientes en estado crítico con LRA que reciben RRT (~36-70% de los pacientes)40,41 y puede asociarse a un mayor riesgo de mortalidad y progresión de la LRA. 42,43
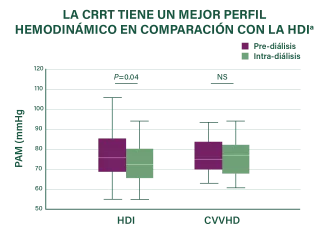
Las pruebas médicas existentes sugieren que la CRRT puede lograr mantener mejor la estabilidad hemodinámica mientras que elimina el fluido en comparación con la hemodiálisis intermitente (HDI) y la diálisis sostenida de baja eficiencia (DSBE).38,44-46
aEnsayo controlado aleatorizado de 80 pacientes adultos en estado crítico con insuficiencia renal aguda que requirieron diálisis en las UCI de un centro de EE. UU. (1995-1999). Los datos corresponden a la terapia de la HDI y la CVVHD durante el día de diálisis inicial. Se muestran los valores medios con rango intercuartílico (límites de cuadro) y valores extremos (margen escaso).38
La CRRT puede ser un tratamiento rentable que puede proporcionar beneficios clínicos y operativos adicionales para pacientes y hospitales.
Rentabilidad de la CRRT
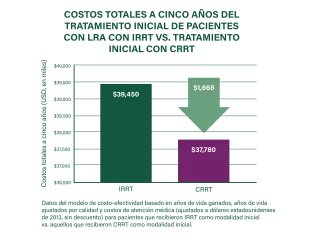
El tratamiento inicial de los pacientes con LRA que utilizan CRRT puede ser más rentable 5 años después del inicio de la RRT que otras modalidades de RRT.3 Un análisis de rentabilidad determinó que la CRRT puede ahorrar aproximadamente $1668 en 5 años (basado en el valor del dólar estadounidense en 2013).3,b,c
Los análisis de rentabilidad indican que la CRRT es rentable en comparación con la RRT intermitente, con la tasa de dependencia de diálisis como el principal impulsor de la rentabilidad.47
bModelo de años de vida ganados, años de vida ajustados por la calidad y costos sanitarios (inflados al valor del dólar estadounidense de 2013, sin descuento) para pacientes que reciben RRT intermitente como modalidad inicial frente aquellos que reciben CRRT como modalidad inicial. Tanto para la CRRT inicial como para la RRT intermitente, la proporción dependiente del tiempo de supervivientes a LRA que se volvieron dependientes de diálisis se ajustó a partir del estudio de Wald et al. (Crit Care Med. 2014; 42:868–877).3
cEl modelo de rentabilidad solo tuvo en cuenta el costo de la implementación de CRRT o RRT intermitente en la UCI, el costo diario de la independencia de la diálisis y el costo diario de la dependencia de la diálisis en el entorno ambulatorio.3
Beneficio del soporte de órganos integrados de un solo sistema
La CRRT se puede combinar con otras terapias de apoyo de órganos en una única plataforma, lo que permite el tratamiento integrado de pacientes con disfunción multiorgánica.37
Un informe de consenso del 17.º grupo de trabajo de la Iniciativa para la Calidad de la Enfermedad Aguda (Acute Disease Quality Initiative, ADQI) afirma que “en situaciones en las que se requieren otras terapias extracorpóreas, se recomienda la CRRT y se prefieren los sistemas integrados a los sistemas paralelos”.37
Episodio 1: Cómo decidir cuándo y quién debe comenzar la diálisis aguda: De la evidencia a la práctica clínica
Presentado por Ravi Mehta, UC San Diego, con Marlies Ostermann, Guy’s and St. Thomas’ Foundation Trust
Episodio 2: Maximización de la vida útil del filtro durante la CRRT: Mejores prácticas en el uso de anticoagulación y citrato
Presentado por Ravi Mehta, UC San Diego, con Ashita Tolwani, Universidad de Alabama en Birmingham
Episodio 3: Cómo desarrollar un programa de calidad de atención de diálisis aguda: Métricas de calidad y mejora continua
Presentado por Ravi Mehta, UC San Diego, con Theresa Mottes, Baylor College of Medicine
Información importante
Vantive, PrisMax son marcas registradas de Vantive Health LLC o sus filiales.
Referencias
-
Ostermann M, Joannidis M, Pani A, et al. Patient selection and timing of continuous renal replacement therapy. Blood Purif. 2016;42(3):224-237.
-
Acute Dialysis Quality Initiative (ADQI) 17 Workgroup. ADQI 17 Figures. 2016. Accessed July 8, 2024.
-
Koyner JL, Mackey RH, Echeverri J, et al. Dialysis dependence at 90 days post discharge for patients treated with continuous renal replacement therapy (CRRT) vs. intermittent hemodialysis (IHD). Poster presented at: 28th International Conference on Advances in Critical Care Nephrology – AKI & CRRT 2023; March 29 - April 1, 2023; San Diego, California, USA.
-
Naorungroj T, Neto AS, Wang A, Gallagher M, Bellomo R. Renal outcomes according to renal replacement therapy modality and treatment protocol in the ATN and RENAL trials. Crit Care. 2022;26:269.
-
Ethgen O, Schneider AG, Bagshaw SM, Bellomo R, Kellum JA. Economics of dialysis dependence following renal replacement therapy for critically ill acute kidney injury patients. Nephrol Dial Transplant. 2015;30(1):54-61.
-
Wald R, Gaudry S, da Costa BR, et al. Initiation of continuous renal replacement therapy versus intermittent hemodialysis in critically ill patients with severe acute kidney injury: a secondary analysis of STARRT-AKI trial. Intensive Care Med. 2023;49(11):1305-1316.
-
Ethgen O, Murugan R, Echeverri J, Blackowicz M, Harenski K, Ostermann M. Economic analysis of renal replacement therapy modality in acute kidney injury patients with fluid overload. Crit Care Explor. 2023;5(6):e0921.
-
KDIGO Acute Kidney Injury Work Group. KDIGO Clinical Practice Guideline for Acute Kidney Injury. Kidney Int Suppl. 2012;2(1):1-138.
-
Aglae C, Muller L, Reboul P, et al. Heterogeneity of cause, care, and prognosis in severe acute kidney injury in hospitalized patients: a prospective observational study. Can J Kidney Health Dis. 2019;6.
-
Cerdá J, Lameire N, Eggers P, et al. Epidemiology of acute kidney injury. Clin J Am Soc Nephrol. 2008;3(3):881-886.
-
Kellum JA, Sileanu FE, Bihorac A, Hoste EA, Chawla LS. Recovery after acute kidney injury. Am J Respir Crit Care Med. 2017;195(6):784-791.
-
Chawla L, Bellomo R, Bihorac A, et al. Acute kidney disease and renal recovery: consensus report of the Acute Disease Quality Initiative (ADQI) 16 Workgroup. Nat Rev Nephrol. 2017;13:241-257.
-
Mehta S, Chauhan K, Patel A, et al. The prognostic importance of duration of AKI: a systematic review and meta-analysis. BMC Nephrol. 2018;19(1):91.
-
Nisula S, Kaukonen KM, Vaara ST, et al. Incidence, risk factors and 90-day mortality of patients with acute kidney injury in Finnish intensive care units: the FINNAKI study. Intensive Care Med. 2013;39:420-428.
-
Melo FAF, Macedo E, Fonseca Bezerra AC, et al. A systematic review and meta-analysis of acute kidney injury in the intensive care units of developed and developing countries. PLoS One. 2020;15(1):e0226325.
-
Jiang L, Zhu Y, Luo X, et al. Epidemiology of acute kidney injury in intensive care units in Beijing: the multi-center BAKIT study. BMC Nephrol. 2019;20:468.
-
Bouchard J, Acharya A, Cerda J, et al. A prospective international multicenter study of AKI in the intensive care unit. Clin J Am Soc Nephrol. 2015;10(8):1324-1331.
-
Uchino S, Kellum JA, Bellomo R, et al. Acute renal failure in critically ill patients: a multinational, multicenter study. JAMA. 2005;294(7):813-818.
-
De Corte W, Dhondt A, Vanholder R, et al. Long-term outcome in ICU patients with acute kidney injury treated with renal replacement therapy: a prospective cohort study. Crit Care. 2016;20:256.
-
Garzotto F, Ostermann M, Martín-Langerwerf D, et al. The Dose Response Multicentre Investigation on Fluid Assessment (DoReMIFA) in critically ill patients. Crit Care. 2016; 20:196.
-
Gammelager H, Christiansen CF, Johansen MB, Tønnesen E, Jespersen B, Sørensen HT. Three-year risk of cardiovascular disease among intensive care patients with acute kidney injury: a population-based cohort study. Crit Care. 2014;18(5):492.
-
Go AS, Hsu C, Yang JT, et al. Acute kidney injury and risk of heart failure and atherosclerotic events. Clin J Am Soc Nephrol. 2018;13(6):833-841.
-
Wu V, Wu C, Huang T, et al. Long-term risk of coronary events after AKI. J Am Soc Nephrol. 2014;25(3):595-605.
-
Wu VC, Wu PC, Wu CH, et al. The impact of acute kidney injury on the long-term risk of stroke. J Am Heart Assoc. 2014;3(4):e000933.
-
Brown JR, Parikh C, Ross C, et al. Impact of perioperative acute kidney injury as a severity index for thirty-day readmission after cardiac surgery. Ann Thorac Surg. 2014;97(1)111-117.
-
Brown JR, Hisey W, Marshall E, et al. Acute kidney injury severity and long-term readmission and mortality after cardiac surgery. Ann Thorac Surg. 2016;102(5):1482-1489.
-
Lai TS, Wang CY, Pan SC, et al. Risk of developing severe sepsis after acute kidney injury: a population-based cohort study. Crit Care. 2013;17:R231.
-
Horkan CM, Purtle SW, Mendu ML, Moromizato T, Gibbons FK, Christopher KB. The association of acute kidney injury in the critically ill and postdischarge outcomes: a cohort study. Crit Care Med. 2015;43(2):354-364.
-
Koulouridis I, Price LL, Madias NE, Jaber BL. Hospital-acquired acute kidney injury and hospital readmission: a cohort study. Am. J. Kidney Dis. 2015;65(2)275-282.
-
Sawhney S, Marks A, Fluck N, et al. Acute kidney injury as an independent risk factor for unplanned 90-day hospital readmissions. BMC Nephrol. 2017;18:9.
-
Silver SA, Harel Z, McArthur E, et al. 30-day readmissions after an acute kidney injury hospitalization. Am J Med. 2017;130(2)163-172.
-
Coca SG, Yusuf B, Shlipak MG, Garg AX, Parikh CR. Long-term risk of mortality and other adverse outcomes after acute kidney injury: a systematic review and meta-analysis. Am J Kidney Dis. 2009; 53(6):961-973.
-
See EJ, Jayasinghe K, Glassford N, et al. Long-term risk of adverse outcomes after acute kidney injury: a systematic review and meta-analysis of cohort studies using consensus definitions of exposure. Kidney Int. 2019;95(1):160-172.
-
Srisawat N, Sileanu FE, Murugan R, et al. Variation in risk and mortality of acute kidney injury in critically ill patients: a multicenter study. Am J Nephrol. 2015;41(1):81-88.
-
Hoste EA, Bagshaw SM, Bellomo R, et al. Epidemiology of acute kidney injury in critically ill patients: the multinational AKI-EPI study. Intensive Care Med. 2015;41(8):1411-1423.
-
Coca SG, Singanamala S, Parikh CR. Chronic kidney disease after acute kidney injury: a systematic review and meta-analysis. Kidney Int. 2012;81(5):442-448.
-
Ronco C, Ricci Z, De Backer D, et al. Renal replacement therapy in acute kidney injury: controversy and consensus. Crit Care. 2015;19(1):146.
-
Nadim MK, Forni LG, Bihorac A, et al. Cardiac and vascular surgery-associated acute kidney injury: the 20th international consensus conference of the ADQI (Acute Disease Quality Initiative) group. J Am Heart Assoc. 2018;7(11):e008834.
-
Augustine JJ, Sandy D, Seifert TH, Paganini EP. A randomized controlled trial comparing intermittent with continuous dialysis in patients with ARF. Am J Kidney Dis. 2004;44(6):1000-1007.
-
Bouchard J, Soroko SB, Chertow GM, et al. Fluid accumulation, survival and recovery of kidney function in critically ill patients with acute kidney injury. Kidney Int. 2009;76(4):422-427.
-
Clark WR, Ding X, Qiu H, et al. Renal replacement therapy practices for patients with acute kidney injury in China. PLoS One. 2017;12(7):e0178509.
-
STARRT-AKI Investigators; Canadian Critical Care Trials Group; Australian and New Zealand Intensive Care Society Clinical Trials Group. Timing of initiation of renal-replacement therapy in acute kidney injury. N Engl J Med. 2020;383(5):502.
-
Izawa J, Kitamura T, Iwami T, et al. Early-phase cumulative hypotension duration and severe-stage progression in oliguric acute kidney injury with and without sepsis: an observational study. Crit Care. 2016;20:405.
-
Haase-Fielitz A, Haase M, Bellomo R, et al. Perioperative hemodynamic instability and fluid overload are associated with increasing acute kidney injury severity and worse outcome after cardiac surgery. Blood Purif. 2017;43(4):298-308.
-
Bagshaw SM, Berthiaume LR, Delaney A, Bellomo R. Continuous versus intermittent renal replacement therapy for critically ill patients with acute kidney injury: a meta-analysis. Crit Care Med. 2008;36(2):610-617.
-
Fieghen HE, Friedrich JO, Burns KE, et al. The hemodynamic tolerability and feasibility of sustained low efficiency dialysis in the management of critically ill patients with acute kidney injury. BMC Nephrol. 2010;11:32.
-
Singh A, Hussain S, Kher V, Palmer AJ, Jose M, Antony B. A systematic review of cost-effectiveness analyses of continuous versus intermittent renal replacement therapy in acute kidney injury. Expert Rev Pharmacoecon Outcomes Res. 2022;22(1):27-35.